Produktinformationen
|
Produktname |
Katze. NEIN |
Spez. |
|
Dil Zellmembran-Rotfluoreszenz-Färbekit |
G1705 |
100-1000 T |
Produktbeschreibung/Einführung
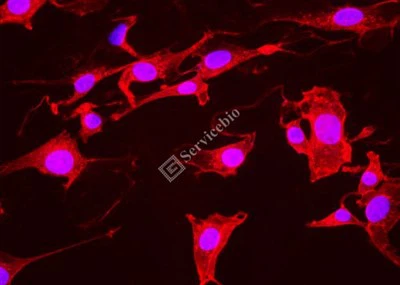
Dil, auch bekannt als DilC18(3), 1,1`-Dioctadecyl-3,3,3`,3`-tetramethylindocarbocyaninperchlorat, mit einem Molekulargewicht von 933,87, ist eine Klasse lipophiler, langkettiger Dialkyldicarbocyanine Farbstoffe, fluoreszierende Farbstoffe, die häufig zur Markierung von Zellmembranen und anderen fettlöslichen biologischen Strukturen verwendet werden. Nach dem Eintritt in die Zellmembran kann Dil seitlich diffundieren und die gesamte Zellmembran allmählich anfärben. Die Fluoreszenz von Dil ist vor dem Eintritt in die Zellmembran sehr schwach, und die Fluoreszenzintensität wird stark erhöht, wenn es an die Zelle bindet, und es kann orangefarbene emittieren. rote Fluoreszenz nach Anregung und kann mit Standard-TRITC-Filtern nachgewiesen werden. Die maximale Anregungswellenlänge von Dil beträgt 550 nm und die maximale Emissionswellenlänge beträgt 564 nm. Aufgrund der Eigenschaften von Dil kann es sowohl lebende als auch fixierte Zellen färben. Zusätzlich. Dil-Sonden haben im Allgemeinen keinen Einfluss auf die Lebensfähigkeit von Zellen, daher können vorwärts oder rückwärts markierte Zellen oder einige Substanzen (Exosomen) als Tracer-Nachweis verwendet werden.
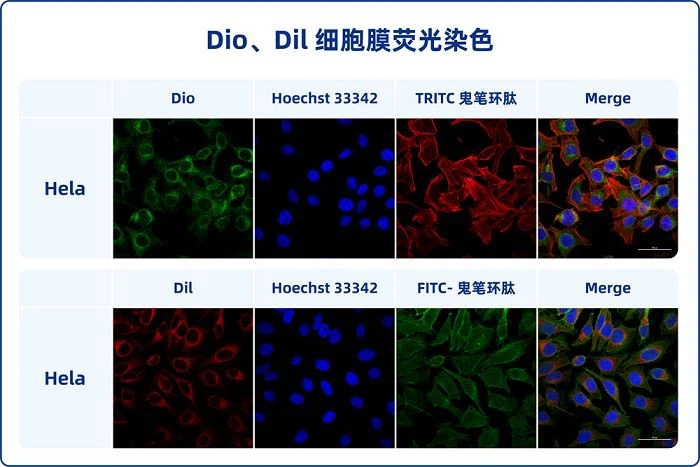
Das Dil-Zellmembran-Rotfluoreszenz-Färbekit enthält eine Dil-Fluoreszenzsonde und einen optimierten Färbepuffer, der die Zellmembranfärbung schneller und die Fluoreszenz heller und stabiler machen kann.
Lager- und Versandbedingungen
Mit Trockeneis versenden; Bei -20 Grad im Dunkeln lagern, 6 Monate gültig.
Produktinhalte
|
Komponentennummer |
Komponente |
G1704 |
|
G1705-1 |
Dil Cell Membrane Rot fluoreszierende Sonde |
100μL |
|
G1705-2 |
Färbepuffer |
100 ml |
|
Handbuch |
Ein Exemplar |
|
Testprotokoll/-verfahren
1. Vorbereitung der Dil-Färbe-Arbeitslösung:
1.1. Mischen und verdünnen Sie Dil Cell Membrane Red Fluorescent Probe mit Färbepuffer im Verhältnis 1:250, um die Dil Färbe-Arbeitslösung (gebrauchsfertig) herzustellen. Beachten Sie, dass das Verdünnungsverhältnis der Dil-Sonde je nach Situation auf 1:250-1:500 eingestellt werden kann, um den besten Färbeeffekt zu erzielen.
2. Färbung lebender Suspensionszellen
2.1. Zentrifugieren Sie die suspendierten Zellen bei 500-1,000×g bei Raumtemperatur für 3-5 min, entfernen Sie den Zellüberstand;
2.2. Fügen Sie die entsprechende Menge Dil-Färbearbeitslösung hinzu, um die Zellen auf eine endgültige Zelldichte von 1-2×106 Zellen/ml zu resuspendieren.
2.3. Bei 37 Grad im Dunkeln für 5-20 Minuten inkubieren. Die optimale Inkubationszeit variiert für verschiedene Zellen. Beginnen Sie mit 5 Minuten und optimieren Sie die Inkubationszeit basierend auf dem endgültigen Färbeergebnis.
2.4. Am Ende der Inkubation bei 500-1000 g für 3-5 Min. bei Raumtemperatur zentrifugieren und die Dil-Färbe-Arbeitslösung absaugen;
2.5. Die Zellen wurden mit vorgewärmtem PBS oder Zellkulturmedium bei 37 Grad resuspendiert und bei 500-1000 g für 3-5 Minuten zentrifugiert, um den Überstand zu entfernen;
2.6. Wiederholen Sie Schritt 2.5.
2.7. Wird direkt durch Durchflusszytometrie oder durch Fluoreszenzmikroskopie nach Übertragung der Zellen auf eine Multiwellplatte, eine Zellkulturschale oder einen Zellkletterobjektträger nachgewiesen. Dil hat ein Anregungsmaximum bei 550 nm und ein Emissionsmaximum bei 564 nm.
3. Färbung lebender adhärenter lebender Zellen (6-Well-Platte als Beispiel):
3.1. Anhaftende Zellen in einer 6-Wellplatte mit einer bestimmten Dichte aussäen.
3.2. Entfernen Sie das Kulturmedium und waschen Sie die Zellen zweimal mit PBS (empfohlen G4202). Fügen Sie 1 ml Dil-Färbearbeitslösung hinzu (Wellplatten anderer Größe, entsprechend angepasst, um sicherzustellen, dass der Farbstoff die Zellen bedeckt);
3.3. Bei 37 Grad im Dunkeln 5-20min lang inkubieren. Die optimale Inkubationszeit variiert für verschiedene Zellen. Beginnen Sie mit 5 Minuten und optimieren Sie die Inkubationszeit basierend auf dem endgültigen Färbeergebnis.
3.4. Die Arbeitslösung zur Zellmembranfärbung absaugen und die Zellen 1-2 Mal mit vorgewärmtem PBS oder Zellmedium waschen.
3.5. Vorgewärmtes Zellkulturmedium oder Zellmedium bei 37 Grad zugeben und Zellen mittels Fluoreszenzmikroskopie nachweisen. Dil hat ein Anregungsmaximum bei 550 nm und ein Emissionsmaximum bei 564 nm.
4. Färbung fixierter adhärenter Zellen:
4.1. Probenvorverarbeitung:
Für Zellen: Entfernen Sie das Zellmedium und waschen Sie 1-2 Mal mit PBS. Fügen Sie 4 % Paraformaldehyd-Fixierlösung (empfohlen G1101) für 10 Minuten bei Raumtemperatur hinzu. Entfernen Sie die Fixierlösung und waschen Sie 2-3 Mal mit PBS;
4.2. Permeabilisierung: 0.1-0,5 % Triton-100 (hergestellt mit PBS) hinzufügen und 10 Minuten bei Raumtemperatur permeieren lassen. Entfernen Sie die Permeabilisierungslösung und waschen Sie 2-3 Mal mit PBS.
4.3. (Optional, Immunfluoreszenzmarkierung) Mit Antikörpern gemäß Immunfärbungsprotokoll oder mit anderen Farbstoffen inkubieren.
Hinweis: Blockierungslösung, Antikörperverdünnungsmittel und Waschlösung für die Immunfärbung sollten keine Detergenzien enthalten.
4.4. Geben Sie eine angemessene Menge der Dil-Färbe-Arbeitslösung hinzu, um die Zellen zu bedecken, inkubieren Sie bei 37 Grad ohne Licht für 5-20 Minuten und saugen Sie die Dil-Färbe-Arbeitslösung ab. Um optimale Färbeergebnisse zu erzielen, wird empfohlen, die Färbezeit an die jeweilige Zellprobe anzupassen.
4.5. Die Zellen wurden 2-3 Mal mit PBS gewaschen und dann zur Beobachtung unter ein Fluoreszenzmikroskop gestellt (Zellen müssen mit einer entsprechenden Menge PBS bedeckt sein). Dil hat eine maximale Anregungswellenlänge von 550 nm und eine maximale Emissionswellenlänge von 564 nm .
5. Fluoreszenzmarkierung von Exosomen:
5.1. Resuspendierte Exosomenfällung mit einer geeigneten Menge Dil-Färbearbeitslösung.
5.2. 30 Minuten lang im Dunkeln bei 37 Grad inkubieren.
5.3. (optional) Verdünnen Sie die Probe mit dem 10-fachen Volumen an PBS.
5.4. Extrahierte Exosomen erneut gemäß dem vorherigen Extraktionsprotokoll, um überschüssige Farbstoffe zu entfernen.
5.5. Sammeln Sie den Niederschlag der Exosomen und resuspendieren Sie ihn in PBS, um Dil-markierte Exosomen zu erhalten. Es kann für nachfolgende Experimente, beispielsweise zur zellulären Aufnahme, verwendet werden.
Notiz
1. Alle fluoreszierenden Farbstoffe haben Probleme mit der Löschung. Bitte schützen Sie sie während des Betriebs vor Licht, um die Fluoreszenzlöschung zu verlangsamen.
2. Da die Sonde lipophil ist, vermeiden Sie bitte die Verwendung von Reagenzien, die Glycerin oder andere organische Stoffe enthalten.
3. Wenn eine Fixierung erforderlich ist, empfehlen wir die Fixierung in 4 % Paraformaldehyd. Andere ungeeignete Fixierlösungen führen zu einem hohen Fluoreszenzhintergrund.
4. Das optimale Verdünnungsverhältnis und die optimale Inkubationszeit der Sonde sollten aufgrund der unterschiedlichen Empfindlichkeit zwischen Zellen und experimentellen Anforderungen an die tatsächliche Situation angepasst werden.
5. Zu Ihrer Sicherheit und Gesundheit tragen Sie bitte eine Schutzbrille, Handschuhe oder Schutzkleidung.
Nur für Forschungszwecke!
Beliebte label: Dil-Zellmembran-Rot-Fluoreszenz-Färbekit, China Dil-Zellmembran-Rot-Fluoreszenz-Färbekit Hersteller, Lieferanten, Fabrik